
Opis badania: Choroba Leśniowskiego-Crohna (ChL-C) należy do nieswoistych zapaleń jelit, chorób o przewlekłym charakterze, przebiegającymi z okresami zaostrzeń i remisji. Etiologia ChL-C nie została dokładnie poznana; jest wypadkową predyspozycji genetycznych, zaburzeń immunologicznych i czynników środowiskowych. Zmiany zapalne w ChL-C obejmują całą grubość ściany przewodu pokarmowego i mogą dotyczyć całego przewodu pokarmowego: od jamy ustnej po odbyt. Lokalizacja zmian zapalnych w przełyku, żołądku i dwunastnicy w populacji pediatrycznej występuje u 30% pacjentów i jest jednym z czynników złego rokowania w ChL-C. Innym, znanym czynnikiem złego rokowania w ChL-C jest wiek pacjenta w chwili rozpoznania choroby: im młodszy, tym gorsze rokowanie.
Leczenie ChL-C jest przewlekłe i trudne. Obejmuje leczenie dietetyczne, farmakologiczne i chirurgiczne. W leczeniu farmakologicznym zastosowanie znajdują leki stosowane ogólnie: preparaty 5-ASA, leki immunomodulacyjne, leki biologiczne, oraz preparaty stosowane miejscowo: czopki, wlewki, kapsułki o przedłużonym uwalnianiu. Optymalne leczenie polega na połączeniu leków działających ogólnie i miejscowo – w zajętym zmianami chorobowymi odcinku jelita. W miejscowym leczeniu ChL-C największe znaczenie odgrywa budezonid, kortykosteroid o silnym działaniu przeciwzapalnym. Charakteryzuje się bardzo małą biodostępnością, w 90% rozkłada się w wątrobie; oznacza to, że jedynie 10% leku przechodzi do krążenia systemowego i może wywoływać działania niepożądane. Obecnie, budezonid znajduje zastosowanie w leczeniu zmian zapalnych zlokalizowanych w końcowym odcinku jelita cienkiego (kapsułki o przedłużonym uwalnianiu lub kapsułki dojelitowe), zmian zapalnych zlokalizowanych w odbytnicy i esicy (doodbytnicza pianka), zmian zapalnych zlokalizowanych w jelicie grubym. Niestety brak jest zupełnie leczenia miejscowego dla pacjentów z ChL-C ze zmianami zlokalizowanymi w przełyku, żołądku i dwunastnicy. Zalecenia sugerują rozważenie zastosowania leków zobojętniających np. inhibitorów pompy protonowej (IPP), co najczęściej nie powoduje remisji zmian zapalnych a jedynie zmniejszenie objawów.
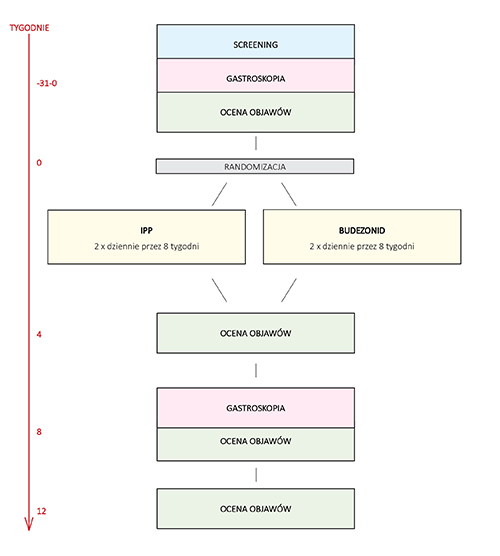
W związku z powyższym postawiono hipotezę, że w przypadku zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy u dzieci z ChL-C dołączenie do leczenia ogólnego miejscowo działającego budezonidu może być skuteczne. Celem niniejszego badania jest ocena skuteczności miejscowo stosowanego budezonidu w leczeniu zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy u dzieci z ChL-C. Badanie to jest badaniem prospektywnym, z randomizacją, z pojedynczo ślepą próbą, pojedynczo pozorowane zostanie przeprowadzone w 3 akademickich szpitalach zajmujących się diagnostyką i leczeniem dzieci z ChL-C w Warszawie, Krakowie i Poznaniu. Wszystkie preparaty dzieci będą przyjmować doustnie, co 12 godzin, przez 8 tygodni. Dziecko będzie połykać kapsułkę/kapsułki (z omeprazolem) popijając ją wodą lub zawartość ampułki/ampułek (budezonidu). Przez 30 minut po połknięciu każdej dawki pacjent nie będzie pił, jadł, żuł gumy ani mył zębów. Po 30 minutach pacjent będzie proszony o wypłukanie ust. Przewidywany czas od rozpoczęcia screeningu do momentu randomizacji wynosi 2 tygodnie. Wizyty kontrolne będą odbywały się w 4, 8 i 12 tygodniu trwania badania. Dozwolone odstępstwo od wyznaczonych punktów kontrolnych (w tym randomizacji) wynosi +/- 4 dni.
Cele badania: Celem niniejszego badania jest ocena skuteczności miejscowo stosowanego budezonidu w leczeniu zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy u dzieci z ChL-C.
Grupa badania: Zakładając moc testu 90% i błąd alfa 5%, do badania należy włączyć 114 pacjentów: po 57 w każdej grupie. Zakładając, że 20% pacjentów może nie ukończyć badania, ostateczna wielkość grupy wynosi 138 pacjentów (w każdej grupie 69 pacjentów). W związku z powyższym postawiono hipotezę, że w przypadku zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy u dzieci z ChL-C dołączenie do leczenia ogólnego miejscowo działającego budezonidu może być skuteczne.
Stan realizacji Projektu: marzec 2025
Monitorem badania jest Alina Zuzanna Łuczak
Badanie BETHESDA jest w trakcie realizacji i obecnie aktywnie rekrutuje pacjentów w 2 ośrodkach badawczych.
Uniwersytecki Szpital Dziecięcy w Krakowie
Liczba zrekrutowanych osób: 3
Liczba osób do zrekrutowania: 44
Kontakt do ośrodka:
Kraków, ul. Wielicka
telefon: 12 333 93 30,
email: kinga.kowalska-duplaga@uj.edu.pl
Uniwersyteckie Centrum Kliniczne Warszawskiego Uniwersytetu Medycznego
Liczba zrekrutowanych osób: 8
Liczba osób do zrekrutowania: 50
Kontakt do ośrodka:
Warszawa, ul. Żwirki i Wigury 63a
telefon: 22 57 20 014,
email: abanaszkiewicz@wum.edu.pl
Trwa proces uruchomienia kolejnego ośrodka badawczego.
Udział w badaniu jest możliwy dla pacjentów spełniających poniższe kryteria:
Kryteria włączenia pacjentów:
- wiek 6-18 lat;
- ChL-C rozpoznana wg powszechnie przyjętych kryteriów z Porto uwzględniających kryteria kliniczne, endoskopowe i histopatologiczne;
- zmiany zapalne w przełyku i/lub żołądku i/lub dwunastnicy stwierdzone w badaniu endoskopowym i/lub w badaniu histopatologicznym (w skali Paryskiej aktywność ChL-C: L4a, czyli zajęcie górnego odcinka przewodu pokarmowego do więzadła Treitza);
- w przypadku wykorzystania wcześniejszego badania - wynik histopatologiczny nie może być starszy niż 31 dni przed randomizacją pacjenta;
- stabilne, rozumiane jako brak modyfikacji leczenia, leczenie ChL-C przez ≥2 tyg
- wykluczenie innych, poza ChL-C, przyczyn zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy takich jak: refluksowe zapalenie przełyku, opryszczkowe zapalenie przełyku, cytomegalowirusowe zapalenie przełyku, eozynofilowe zapalenie przełyku i(lub) żołądka i(lub) dwunastnicy, zakażenie Helicobacter pylori;
- świadoma zgoda rodziców lub opiekunów dziecka na udział w badaniu; w przypadku dzieci ≥ 13 r.ż. dodatkowo zgoda dziecka biorącego udział w badaniu.
- deklaracja wstrzemięźliwości seksualnej podczas całego udziału w badaniu.
Kryteria wyłączenia
- inne, poza ChL-C, przyczyny zmian zapalnych w przełyku i/lub żołądku i/lub dwunastnicy takie jak: refluksowe zapalenie przełyku, opryszczkowe zapalenie przełyku, cytomegalowirusowe zapalenie przełyku, eozynofilowe zapalenie przełyku i(lub) żołądka i(lub) dwunastnicy, zakażenie Helicobacter pylori;
- stosowanie steroidów ogólnie lub wziewnie, IPP do 30 dni przed włączeniem do badania;
- ostre zakażenie wirusowe lub bakteryjne do 30 dni przed włączeniem do badania;
- poranny kortyzol <5 ug/dl;
- brak świadomej zgody rodziców lub opiekunów dziecka na udział w badaniu; w przypadku dzieci ≥13 r.ż. brak zgody dziecka na udział w badaniu.
- ciąża pacjentki; karmienie piersią; brak zgody kobiety w wieku rozrodczym lub mężczyzny płodnego do stosowania zaleceń dotyczących antykoncepcji w trakcie badania;
- przebyta choroba nowotworowa u pacjenta.
Badanie zostało zarejestrowane w specjalistycznych bazach danych:
https://clinicaltrials.gov/study/NCT06719622?locStr=%3D3
https://euclinicaltrials.eu/search-for-clinical-trials/?lang=pl&EUCT=20…